В момента, терапевтичните възможности включват ефект лечение CHD на клиничните симптоми на заболяването и намаляване на риска от инфаркт на миокарда, сърдечна смърт чрез намаляване на дисбаланса между търсенето на инфаркт на кислород и доставката, превенция на развитието на болестта, възстановяване на коронарния кръвен поток през коронарните артерии ангиопластика или реваскуларизация на миокарда на. Въпреки напредъка в лечението на заболяване на коронарната артерия, процентът на смъртност от това заболяване остава висока, което изисква разработването на нови подходи за лечение на заболяване на коронарната артерия. Генна терапия, по-специално, с използването на ангиогенни растежни фактори е потенциален нов лечение на болест на сърцето. През последните години има множество експериментални изследвания на ангиогенезата фактори, и първите клинични проучвания при пациенти с исхемична болест на сърцето и периферно съдово заболяване [3, 5]. Ангиогенезата е комплексен многостепенен процес на образуване на нови съдове от обещаващ или фрактура (разделяне) на съществуващата [2, 4]. Ангиогенезата се състои от няколко последователни етапа: 1), вазодилатация, 2) на миграцията и адхезията на пролиферацията на ендотелни клетки и 3) се образува трислойна съдовата стена нови васкуларни тръби, които се развива като циркулиращ възстановяване [4]. За образуването на кръвоносни съдове, по-големи от капиляри необходими миграция на гладкомускулни клетки и тяхната адхезия към новообразуваната матрицата на нови съдове. В експеримента, модификация на тези стъпки може да стимулира и инхибира ангиогенезата. Сред редица фактори, участващи в регулацията на ангиогенезата, най-важното е съдов ендотелен растежен фактор VEGF (съдов ендотелен растежен фактор - VEGF) и неговите хомолози, [4]. VEGF, е основен индуктор на ангиогенезата, е гликопротеин, повишава съдовата пропускливост, селективно повлияване на митогенните ефекти върху ендотелни клетки, се произвежда от ендотелните клетки в хипоксични условия [1, 3]. Нивото на експресия на VEGF постепенно намалява след раждане и е минимално в повечето възрастни тъкани, с изключение на местата на активна ангиогенеза - като яйчниците, матката, кожата (растеж на косата) на. Високите нива на VEGF в белите дробове при възрастни могат да бъдат свързани с ендотелна фенестрация [3]. Въпреки VEGF експресия може да бъде активиран при определени условия - като присъствието на миокардна исхемия, възпаление на ретината, тумор [1, 9, 10, 12].
Инфаркт на капилярната мрежа играе важна роля в транспорта на кислород и хранителни вещества до кардиомиоцитите. Повишената капилярна плътност в миокарда осигурява висока активност miokardailnogo притока на кръв, миокардна перфузия и метаболизъм в исхемия. Промяна на система за обмен на плътност и повърхност microcircular капилярен канал може да се индуцира чрез процес на ангиогенеза.
Целта на това проучване е да се изследва влиянието на VEGF-164 върху растежа и развитието, както и повредената състояние gemomikrotsirkulyatsii миокарда, причинени от запушване на предна низходяща клон на коронарната артерия в пери-инфаркт, и отдалечени от фокусни области на миокарда в експеримента.
Експериментите бяха поставени на 22 бял мелези мъжки плъхове с тегло 200-250 грама. Първата група се състои от 6 животни интактни плъхове, втора група (п = 8) - Контролни опитни животни, които произвеждат коронарна оклузия на артерия на peredneniskhodyaschey. Третата група от опитни животни (п = 8) се инжектира интравенозно в предварително VEGF-164 състав при доза от 0.3 мг / кг и произведени оклузия на коронарната артерия.
Получаване VEGF, което представлява полипептид, състоящ се от 164 аминокиселини, се прилага в доза от 0.3 мг / кг, след разтваряне в 1 мл буфер и се центрофугира в продължение на 5 минути. Лекарството се прилага интрамиокардиално.
Експериментална миокардна некроза възпроизведени чрез запушване на лявата предна низходяща коронарна артерия (LCA) в лявата стернотомия под Nembutal анестезия (i.p., 40 мг / кг) в механична вентилация. Преди инжектирането на упойка животните извършват атропин 0.04 m 2 / кг за предотвратяване оток на лигавицата трахеална интубация. Обезглавяване е извършено на 7-ия ден след оклузия при нембуталовата анестезия.
За проучване на морфологично състояние на миокарда използва конвенционалния метод на оцветяване.
Hemomicrocirculatory канал микроскопско проучен на миокарда препарати, третирани с модифициран метод на Gomori S.A.Sisakyanu [7]. С окуляр микрометър измерва средния диаметър на капилярите (г), изчислена плътност (обща дължина - L), капиляри обмен повърхност (DIC) и капацитет на капилярен слой (ERC) за 1 mm 3 инфаркт тъкан.
Статистически анализ се извършва чрез Student Т-критерий.
Нашите данни показват, че на 7-мия ден след оклузията в некротични огнища са открити голям брой некротични клетки и изолирани фрагменти на капилярите, а след прилагане на VEGF съдов отговор е по-силно изразено.
В проучването на микроваскулатурата на миокарда на интактни животни бяха идентифицирани разположени паралелно и равномерно пълни капиляри, както и напречни бразди кардиомиоцити (фиг. 1).

Фиг. 1. миокарда на здрави животни. Разположени паралелно капиляри и напречни бразди на мускулните влакна. 7 х 40.
Контролните животни се характеризират с наличието на множество области на светлина, лишени от съдови елементи. Съседните области на миокардна некроза открити гъсто разположени неравномерно пълни капиляри. В същото време стените на капилярите се оцветяват по-интензивни, много от тях се изви, с неправилни контури. В много области оглед на това е напълно отсъстват напречни бразди на мускулните влакна (фиг. 2). В миокарда на животните, които са получили VEGF открити по-плътна подреждане на капиляри anastomiruyuschih една с друга и образуващи вид на капилярната мрежа в областите, в непосредствена близост до некроза (фиг. 3). В по-отдалечени области на некроза капиляри са успоредни една на друга, като правилният ход с гладки контури.
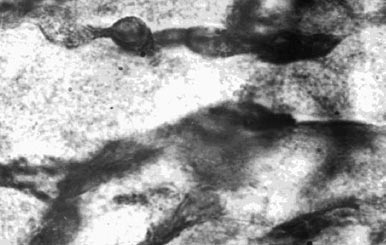
Фиг. 2. запушване на лявата коронарна артерия. Paranecrotic област. Контурите капиляри груб, неравни оцветители стени, капиляри образуват разширяване mikroanevrizmaticheskie. 10 х 40
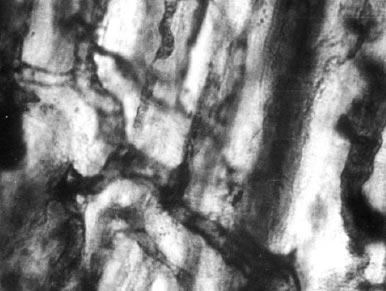
Фиг. 3. Създадена инфаркт на капилярната мрежа в области, съседни на некрозата на ден 7 след оклузия на коронарната артерия. 10 х 40.
почти не се различава от това на контролните животни в рамките на надеждност (3.3%, р> 0.1) при морфометрично система за оценка perinekroticheskoy средните капиляри диаметър капиляри .Otmechalos увеличение плътност функционира капилярна зона (14.7%, р<0,05) и ОПК (12,1 %, р<0,05) в этих участках (табл.1). В более отдаленных отделах миокарда капилляры располагались параллельно друг к другу, их средний диаметр и количество функционирующих капилляров в пределах достоверности не отличались от таковых в перинекротической зоне.
Таблица 1
Морфометрични промени в малки кръвоносни съдове на миокарда perinekroticheskoy оклузия зона и прилагане на LCA зеленчуци
Параметри на миокарда ICR
Забележка: * р <0,05, достоверность разницы с интактными животными; #p <0,01 – достоверность разницы между животными с окклюзией ЛКА и животными, дополнительно получившими VEGF.
В групата от животни, които са получили предварително инжектиране на VEGF-164, споменати по-плътна подреждане на капилярите в perinekroticheskoy зона (нараства с 24,8%, стр<0,01), так и в отдаленных от него участках. Морфометрические измерения показали отсутствие изменения среднего диаметра капилляров от таковых у контрольных крыс (2,8 %, р>0.1), но броят на функциониращите капиляри достигат значително високи стойности в perinekroticheskoy площ (24.8%, р<0,01), так и отдаленных от него участках. Именно благодаря увеличению количества функционирующих капилляров наблюдалось значительное увеличение ОПК (25,1 %, р<0,01).
Един обещаващ посока в експерименталната кардиологията е лечението на миокардна исхемия, неоваскуларизация на сърцето с помощта на така наречените "ангиогенни" медиатори, предизвикващи образуването съд. Инфаркт на ангиогенеза се случва в тялото и може да се стимулира при остра исхемия, исхемично състояние [1, 6]. Процесът на ангиогенеза е придружено от предизвикване на активиране на няколко транскрипционни фактори - Staf 3; SP-1, Pax-5 [4]. Няколко изследвания са показали, че обезпечение съдовата система защита на исхемична миокарда по време на остра коронарна оклузия.
В момента има много нерешени въпроси по отношение на методите за прилагане на VEGF за терапевтично ангиогенезата. Проучванията при прилагането на ангиогенни фактори смесени. В първото проучване показва увеличаване на толерантността към физическо натоварване по време на интракоронарно приложение протеин основен фибробластен растежен фактор (FGF-б) при пациенти над 65 години с тежка ангина. В Revasc рандомизирано проучване, сравняващо 2 групи от пациенти с тежка ангина прилагане VEGF-121 ген, състояща се от аденовирус левокамерната стена след minitoranotomii наблюдава подобрено тест бягаща пътека данни (повишено време преди появата на болка) преди възникване на ST сегмент депресия по-голямо от 1 mm) се наблюдава при 26 седмици [8]. Интравенозно приложение или приложение в "поток дисталния артериалното" ангиогенни растежни фактори могат да предизвикат системни реакции, например, растеж на тумори съд незабелязани, хипотония [2, 3]. Във връзка с това, че е интересен ефект на миокарда инжектиране на VEGF, за да се избегнат редица системни нежелани странични ефекти. Предвид гореизложеното, ние сме тествани в нашите експерименти, той е този метод за въвеждане на VEGF.
Капилярна мрежа играе ключова роля при транспортирането на кислород и енергийни основи кардиомиоцити. Повишената капилярна плътност на миокарда по време на исхемия наблюдава, което показва Физиологичното значение gipoksiindutsirovannogo увеличава ниво ендотелни митогени и техните рецептори [2, 10]. По-специално, след 24 часа. След лигиране на лявата коронарна артерия в експерименталните условия в животински модели показват значително повишаване на нивото на VEGF [12]. Известно е, че активирането на ендогенен VEGF експресия е ранен отговор на миокардна исхемия. Тази реакция се извършва на молекулярно ниво, един от първите механизми за адаптация в миокардна исхемия [1, 3, 13].
В експериментални модели на некроза и ангиогенеза фактор VEGF терапия ние открихме, че терапията активира фактор, наречен процес на ангиогенеза в perinekroticheskoy зона и в отдалечени области на некроза чрез увеличаване на броя на функциониращите капиляри и обменните повърхности на леглото капилярната. Тежестта на съдова реакция на 7-ия ден на експеримента, гъстата подреждането на капилярите и наличието на множество анастомози показващи активиране на циркулация обезпечение perinekroticheskoy зона в контролната група плъхове. Тези промени са адаптивни и адаптивни механизми остра миокардна исхемия и са описани в много експериментални изследвания на моделиране на инфаркт на миокарда и при пациенти с AMI. Един от възможните механизми на тези промени е активирането на ендогенен ангиогенеза в сърцето с редица растежни фактори. Предварителното третиране с VEGF, за разлика от контролните животни, което води до увеличаване на плътността на съдовата система, не само в perinekroticheskoy област, но в области, отдалечени от него.
